Liên hệ:Lỗi Chu (Ông.)
Điện thoại: cộng 86-551-65523315
Di động/WhatsApp: cộng 86 17705606359
Hỏi:196299583
Ứng dụng trò chuyện:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Thêm vào:1002, Hoàng Mao Tòa nhà, Số 105, Mông Thành Đường, Hợp Phì Thành phố, 230061, Trung Quốc
Một năm trước, vào ngày 21 tháng 11 năm 2019, Bristol-Myers Squibb (BMS) thông báo rằng họ đã hoàn thành việc mua lại Celgene trị giá 74 tỷ USD sau khi có sự chấp thuận chống độc quyền từ các chính phủ khác nhau. Theo các điều khoản của thỏa thuận sáp nhập, Celgene trở thành một công ty con thuộc sở hữu của Bristol-Myers Squibb, và công ty mới được niêm yết lại dưới mã chứng khoán BMY.RT. Vào tháng 3 năm 2020, BMS đã thay đổi logo của mình và một thương hiệu mới ra đời. Lần cuối cùng Bristol-Myers Squibb thay đổi logo là vào những năm 1980.
TYK2 là một thành viên của gia đình JAK (các thành viên khác bao gồm JAK1, JAK2 và JAK3), chịu trách nhiệm tham gia ifn-α, IL-6, IL-10 và IL-12 tín hiệu. Gen này chịu trách nhiệm mã hóa tyrosine kinase, cụ thể hơn là một thành viên của họ protein Janus kinase (JAKs). TYK2 có thể phosphorylate IL-12, IL-23, và STAT protein hạ lưu của các thụ thể interferon loại I. Biến thể di truyền của TYK2 có liên quan đến một loạt các bệnh tự miễn dịch.
Ứng cử viên thuốc mới của BMS BMS-986165 (Deucravacitinib) là một đặt cược nặng nề trong lĩnh vực bệnh tự miễn dịch, và nó là tyk2 phát triển nhanh nhất mục tiêu thuốc mới trên thế giới. Sản phẩm này là một loại thuốc công nghệ deuterated ban đầu.
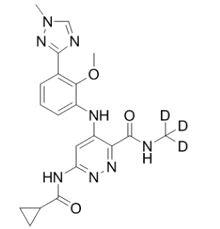
BMS-986165 công thức cấu trúc, một loại thuốc deuterated với một cấu trúc mới
Vào ngày 3 tháng 11 năm 2020, BMS chính thức thông báo rằng BMS-986165 (Deucravacitinib) đã đánh bại giả dược và kiểm soát PED4i dương tính trong một dấu hiệu lâm sàng giai đoạn 3 quan trọng của bệnh vẩy nến có tên POETYK PSO-1 (số đăng ký lâm sàng NCT03624127) Thuốc Apremilast (Apremilast, đã thuộc sở hữu của Amgen). Thử nghiệm lâm sàng này nhằm vào những bệnh nhân bị bệnh vẩy nến mảng bám từ trung bình đến nặng. Tổng cộng có 666 bệnh nhân đã được ghi danh vào các phương pháp điều trị khác nhau, chia thành nhóm thuốc BMS-986165 (Deucravacitinib), nhóm giả dược và nhóm kiểm soát dương tính.
Kết quả của nghiên cứu xác nhận rằng so với giả dược, nhiều bệnh nhân nhận được BMS-986165 (Deucravacitinib) (6 mg, mỗi ngày một lần) trong 16 tuần, đạt được một khu vực bệnh vẩy nến và cải thiện chỉ số mức độ nghiêm trọng ít nhất 75% (PASI 75) và Bác sĩ tĩnh đánh giá các tổn thương da như một toàn thể hoặc gần như loại bỏ (sPGA 0/1). Nghiên cứu lâm sàng POETYK PSO-1 đã đạt đến nhiều điểm cuối chính thứ cấp cùng một lúc. Kết quả cho thấy tỷ lệ bệnh nhân đạt được PASI 75 và sPGA 0/1 sau khi điều trị Deucravacitinib tốt hơn Otezla® (apster) ở tuần 16. Trong nghiên cứu này, kết quả an toàn tổng thể của Deucravacitinib phù hợp với kết quả của nghiên cứu giai đoạn II đã công bố trước đó. Các nhà điều tra chính của thử nghiệm lâm sàng này sẽ tiếp tục cải thiện các thử nghiệm lâm sàng giai đoạn 3 tiếp theo và dữ liệu cụ thể sẽ được tiết lộ trong các hội nghị học thuật có thẩm quyền trong tương lai.